Solicitação para a realização das fases 1 e 2 do estudo clínico da Spintec, contra a Covid-19, foi enviada nesta sexta-feira (30).
A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou neste sábado (31) que recebeu pedido de autorização para o início dos testes em humanos da Spintec, vacina contra a Covid-19 desenvolvida por pesquisadores da Universidade Federal de Minas Gerais (UFMG).
A solicitação para a realização das fases 1 e 2 do estudo clínico foi enviada nesta sexta-feira (30).
De acordo com a UFMG, as duas fases serão desenvolvidas concomitantemente e estão previstas para setembro. A primeira, a ser realizada com cerca de 40 voluntários, tem o objetivo de avaliar a segurança da vacina, para identificar se ela provoca ou não efeitos adversos.
Já a fase 2, que vai reunir 150 a 300 voluntários, busca comprovar a capacidade imunogênica da vacina, isto é, de induzir a geração de anticorpos e células de defesa específicas contra o coronavírus.
Serão convocados voluntários que já tiverem recebido duas doses da vacina Coronavac há pelo menos seis meses. A ideia é avaliar a capacidade de resposta imunológica do organismo à terceira dose de um imunizante.
Segundo a Anvisa, a análise da solicitação "considerará a proposta do estudo, o número de participantes e os dados de segurança obtidos até o momento nos estudos pré-clínicos que são realizados em laboratório e animais".
Antes de o pedido ser formalizado, representantes da agência já tinham realizado reuniões prévias com os desenvolvedores da Spintec para orientações e esclarecimentos. O último encontro foi realizado no dia 14 de junho, quando foram discutidos o andamento dos testes e os aspectos regulatórios a serem observados para a submissão do pedido da pesquisa clínica.
A vacina
O dossiê entregue à Anvisa reúne dados e informações sobre o desempenho da Spintec contra a Covid-19 nos testes pré-clínicos realizados em camundongos humanizados, cujo sistema imune se comporta de forma semelhante ao do ser humano, em hamsters e em primatas.
Segundo a UFMG, os resultados foram positivos: a vacina não gerou efeitos colaterais adversos detectáveis e demonstrou a capacidade de produção de anticorpos tanto para proteína S, na qual ocorre a maioria das mutações do coronavírus, quanto para a N. Além disso, foram identificadas respostas protetoras de linfócitos T.
A expectativa é que a Spintec esteja disponível em 2022, quando toda a população já tiver recebido duas doses de vacina. O objetivo é que a vacina reforce a imunidade das pessoas contra o coronavírus.
A etapa de testes clínicos da Spintec conta com recursos da Prefeitura de Belo Horizonte, que vai repassar R$ 30 milhões até o final do ano à universidade, e de R$ 3 milhões de emendas parlamentares.
A fase 3 dos estudos, que deve ser realizada em escala maior, tem um custo estimado de R$ 300 milhões.
Fonte: G1
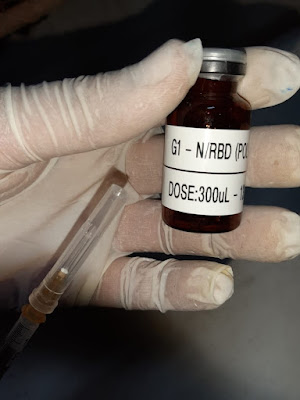
Foto: Flávio Fonseca

Nenhum comentário:
Postar um comentário
COMENTÁRIO SUJEITO A APROVAÇÃO DO MEDIADOR.